Is vaccinatie een goed plan?John Jacobs, 14 november 2020. |
SARS-2 heeft een bijzondere relatie met het afweersysteem. Sommige mensen worden geïnfecteerd, produceren virus, besmetten anderen, maar worden zelf niet ziek. Andere krijgen een afweerreactie en worden grieperig. Een kleine groep heeft een sterke maar minder effectieve afweerreactie die niet leidt tot het neutraliseren van het virus, maar tot een levensbedreigende ziekte. COVID-19 is een virus-gemedieerde immuunpathologie. Immuunpathologie betekent dat de ziekte veroorzaakt wordt door het afweersysteem, in dit geval uitgelokt door virusinfectie. De combinatie van een immuunreactie die te zwak is om het virus op te ruimen en sterk genoeg is om schade te veroorzaken leidt tot paradoxen met mogelijk ernstige gevolgen voor de volksgezondheid.
Afweerparadox
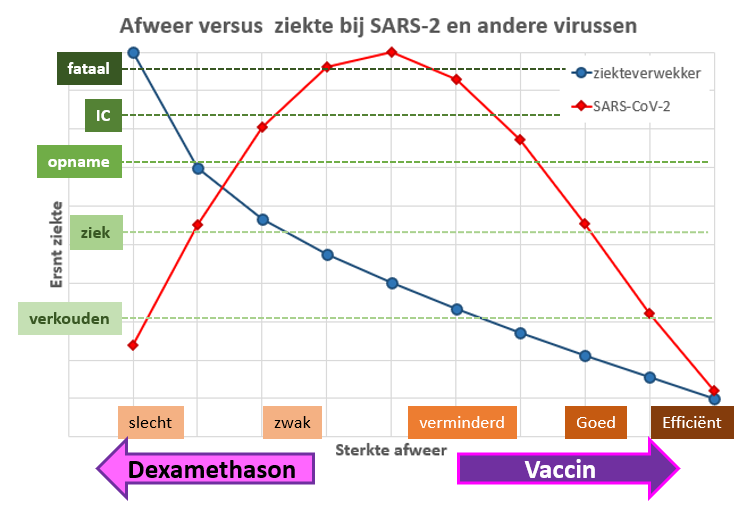
Het afweersysteem biedt goede bescherming tegen de meeste ziekteverwekkers. Meestal geldt: hoe beter de afweer, hoe minder ziek. Die relatie ligt complexer bij SARS-CoV-2 (Figuur 1). Wie efficiënte afweer heeft wordt niet ziek, maar wie een slechte heeft ook niet. Mensen met een verminderde afweer worden het meest ernstig ziek, wie een nog zwakkere afweer heeft wordt minder ziek. Deze paradox is dus het gevolg van de virus-immuunpathologie. Naast de genoemde immuunreactie wordt dit verder geïllustreerd door herinfectie die soms ernstiger is (zie later) en dat de beste therapie voor IC-patiënten met COVID-19 is: onderdrukking van het afweersysteem met dexamethason.
De afweerparadox voor coronavirussen verandert het begrijpen van de ziekte, de behandeling, vaccin-ontwikkeling, maar ook bij strategische overwegingen over testen en bestrijding.
De afweerparadox voor coronavirussen verandert het begrijpen van de ziekte, de behandeling, vaccin-ontwikkeling, maar ook bij strategische overwegingen over testen en bestrijding.
Figuur 1. Afweer versus ziekte bij SARS-2 (rode diamanten) en andere virussen (blauwe cirkel).
Sterk vereenvoudigde een-dimensionele weergave. Voor een meer realistisch beeld van afweer zie COVID en afweer. Dexamethason vermindert de afweer en heeft een positief effect bij COVID-19 patiënten op de IC. Vaccinatie versterkt de afweer en kan voorkomen dat mensen ziek worden. Echter bij mensen met een zwakke afweer zou een vaccin kunnen leiden tot verergering van de ziekte.
Sterk vereenvoudigde een-dimensionele weergave. Voor een meer realistisch beeld van afweer zie COVID en afweer. Dexamethason vermindert de afweer en heeft een positief effect bij COVID-19 patiënten op de IC. Vaccinatie versterkt de afweer en kan voorkomen dat mensen ziek worden. Echter bij mensen met een zwakke afweer zou een vaccin kunnen leiden tot verergering van de ziekte.
Tijdelijke immuniteit
Immuniteit tegen virussen zoals de griep blijft levenslang. Een volgende infectie is met een immunologisch ander virustype (serotype), dat vele mutaties kent ten opzichte van de eerdere stam. Anders wordt het virus geneutraliseerd door de afweer van immune mensen.
Dit verhaal is anders bij coronavirussen. We kennen coronavirussen vooral vanwege hun vermogen om ons elk jaar opnieuw ziek te maken met dezelfde stam. Dezelfde vier corona verkoudheidsvirussen zorgen elk jaar opnieuw voor verkoudheden. Bij SARS-1 en MERS was het aantal besmettingen zo laag dat niemand tweemaal besmet werd. Antistoffen tegen SARS-1 antistoffen blijven niet lang. Overigens zijn antistoffen geen betrouwbare maat voor immuniteit bij SARS-2. Dit is niet onderzocht bij SARS-1.
Herinfectie is niet eenvoudig te bewijzen, omdat beide virusstammen voldoende van elkaar moeten verschillen. Een persoon moet dus op twee verschillende manieren besmet zijn geraakt met twee verschillende viruslijnen. Studies naar bevestigde herinfecties met SARS-2 laten vele gevallen zien inclusief jonge gezonde mensen (Tillet, To, Gupta, Mulder, Larson, Bonifacio, van Elslande, AlFehaidi, Lafaie) en vele reviews (Ledfort, Dao, Kim, Newsweek, BNO news). Herinfecties zijn geen uitzonderingen en het is zorgwekkend dat de tweede infectie meestal niet milder verloopt en vaak zelfs erger.
Ook bij HIV komt herinfectie voor (eigenlijk superinfectie, want de eerste is nog actief). Herinfectie betekent dat de immuniteit na de eerste infectie onvoldoende was of onvoldoende lang bleef. Dat bemoeilijkt ook de ontwikkeling van vaccins die blijven werken. Antistoffen leken bij HIV herinfectie niet te voorkomen, maar eerder juist te versterken.
Gezien het gegeven dat SARS-2 mensen herhaald kan infecteren, is het waarschijnlijk dat dit virus blijft, zoals ook de corona verkoudheidvirussen onder ons blijven. Dan is het belangrijk dat we infecties in mensen kunnen tegengaan door besmettingen te voorkomen met test, traceer en isoleer (TTI) en/of door met vaccinatie te beschermen tegen infectie. Ziekte kan in een vroeg en laat stadium worden behandeld met middelen zoals interferon en dexamethason.
Dit verhaal is anders bij coronavirussen. We kennen coronavirussen vooral vanwege hun vermogen om ons elk jaar opnieuw ziek te maken met dezelfde stam. Dezelfde vier corona verkoudheidsvirussen zorgen elk jaar opnieuw voor verkoudheden. Bij SARS-1 en MERS was het aantal besmettingen zo laag dat niemand tweemaal besmet werd. Antistoffen tegen SARS-1 antistoffen blijven niet lang. Overigens zijn antistoffen geen betrouwbare maat voor immuniteit bij SARS-2. Dit is niet onderzocht bij SARS-1.
Herinfectie is niet eenvoudig te bewijzen, omdat beide virusstammen voldoende van elkaar moeten verschillen. Een persoon moet dus op twee verschillende manieren besmet zijn geraakt met twee verschillende viruslijnen. Studies naar bevestigde herinfecties met SARS-2 laten vele gevallen zien inclusief jonge gezonde mensen (Tillet, To, Gupta, Mulder, Larson, Bonifacio, van Elslande, AlFehaidi, Lafaie) en vele reviews (Ledfort, Dao, Kim, Newsweek, BNO news). Herinfecties zijn geen uitzonderingen en het is zorgwekkend dat de tweede infectie meestal niet milder verloopt en vaak zelfs erger.
Ook bij HIV komt herinfectie voor (eigenlijk superinfectie, want de eerste is nog actief). Herinfectie betekent dat de immuniteit na de eerste infectie onvoldoende was of onvoldoende lang bleef. Dat bemoeilijkt ook de ontwikkeling van vaccins die blijven werken. Antistoffen leken bij HIV herinfectie niet te voorkomen, maar eerder juist te versterken.
Gezien het gegeven dat SARS-2 mensen herhaald kan infecteren, is het waarschijnlijk dat dit virus blijft, zoals ook de corona verkoudheidvirussen onder ons blijven. Dan is het belangrijk dat we infecties in mensen kunnen tegengaan door besmettingen te voorkomen met test, traceer en isoleer (TTI) en/of door met vaccinatie te beschermen tegen infectie. Ziekte kan in een vroeg en laat stadium worden behandeld met middelen zoals interferon en dexamethason.
Vaccinatie-paradox
Het afweersysteem is geëvolueerd om virussen te neutraliseren door natuurlijke afweer, antistoffen en cellulaire immuniteit. Virussen zijn echter met verschillende strategieën geëvolueerd om te ontsnappen aan de neutralisatie door het afweersysteem voordat ze de volgende persoon kunnen infecteren. Dankzij vaccins en hygiëne heeft de mens veel infectieziekten overwonnen. Sommige vaccins voorkomen de infectie en de meeste vaccins verminderen de ernst van ziekte. Vaak gaan beide samen en in het algemeen geldt: hoe sterker de afweerreactie, hoe minder ziek.
Een uitzondering zijn ziektes veroorzaakt door coronavirussen, flavivirussen en HIV. Hier blijken vaccins vaak niet effectief, zelfs niet als sterke afweerreacties worden opgewekt. Een enkel coronavaccin verergerde zelfs het ziekteverloop na infectie door die sterke afweer. Een redelijk sterke afweerreactie tegen SARS-2 maakt ziek, terwijl de virusinfectie blijft. Het vaccin versterkt de afweerreactie tegen het virus. Dit lijkt gewenst bij mensen met een zwakke afweer, maar kan ook leiden tot verergering van de ziekte.
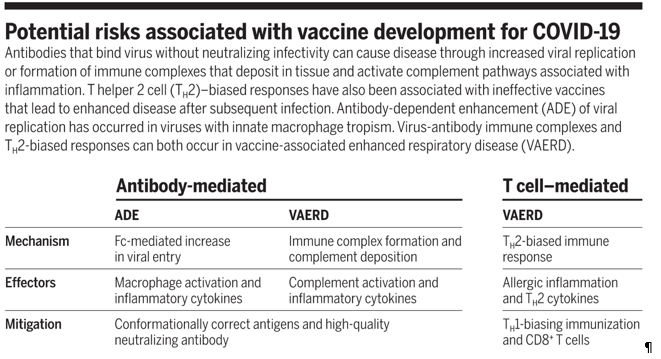
Immunologen wezen in een vroeg stadium erop dat COVID-19 vaccinatie tegengestelde effecten kan hebben. Specifiek genoemd werden antistof-gemedieerde versterking van virusinfectie (ADE) en vaccin-geïnduceerde verergering van longziekte door immuuncomplex-formatie en complement-depositie (VAERD) (Figuur 2). Beide zijn geen directe gevolgen van het vaccin, maar kunnen optreden als een gevaccineerd persoon geïnfecteerd wordt. In dat geval zou het vaccin het tegengestelde doen van wat de bedoeling is: gevaccineerde mensen worden zieker na infectie. Het zieker worden bij een SARS-2 herinfectie lijkt een voorafschaduwing hiervan.
Mogelijk wordt ADE veroorzaakt door de neutraliserende antistoffen tegen het corona Spike eiwit. Dat eiwit zit in alle coronavaccins. De rol van neutraliserende antistoffen in ADE is ook aangetoond bij de coronavirussen SARS-1 en MERS. ADE speelt ook een belangrijke rol bij flavivirussen Dengue-, Zika- en West-Nijl virus, en ook bij HIV (Aidsvirus). ADE bemoeilijkt de ontwikkeling van veilige en effectieve vaccins, en voor al de meeste van deze virussen zijn nog geen werkende vaccins geregistreerd (SARS-1, MERS, HIV, West-Nijl, Zika-virus). De enige uitzondering is Dengue virus.
Een uitzondering zijn ziektes veroorzaakt door coronavirussen, flavivirussen en HIV. Hier blijken vaccins vaak niet effectief, zelfs niet als sterke afweerreacties worden opgewekt. Een enkel coronavaccin verergerde zelfs het ziekteverloop na infectie door die sterke afweer. Een redelijk sterke afweerreactie tegen SARS-2 maakt ziek, terwijl de virusinfectie blijft. Het vaccin versterkt de afweerreactie tegen het virus. Dit lijkt gewenst bij mensen met een zwakke afweer, maar kan ook leiden tot verergering van de ziekte.
Immunologen wezen in een vroeg stadium erop dat COVID-19 vaccinatie tegengestelde effecten kan hebben. Specifiek genoemd werden antistof-gemedieerde versterking van virusinfectie (ADE) en vaccin-geïnduceerde verergering van longziekte door immuuncomplex-formatie en complement-depositie (VAERD) (Figuur 2). Beide zijn geen directe gevolgen van het vaccin, maar kunnen optreden als een gevaccineerd persoon geïnfecteerd wordt. In dat geval zou het vaccin het tegengestelde doen van wat de bedoeling is: gevaccineerde mensen worden zieker na infectie. Het zieker worden bij een SARS-2 herinfectie lijkt een voorafschaduwing hiervan.
Mogelijk wordt ADE veroorzaakt door de neutraliserende antistoffen tegen het corona Spike eiwit. Dat eiwit zit in alle coronavaccins. De rol van neutraliserende antistoffen in ADE is ook aangetoond bij de coronavirussen SARS-1 en MERS. ADE speelt ook een belangrijke rol bij flavivirussen Dengue-, Zika- en West-Nijl virus, en ook bij HIV (Aidsvirus). ADE bemoeilijkt de ontwikkeling van veilige en effectieve vaccins, en voor al de meeste van deze virussen zijn nog geen werkende vaccins geregistreerd (SARS-1, MERS, HIV, West-Nijl, Zika-virus). De enige uitzondering is Dengue virus.
Figuur 2. Mogelijk risico's van COVID-19 vaccins. ADE is infectie door antistoffen. VAERD is lokale ontstekingsreacties in de longen door immuuncomplexen van virus en antistoffen.
Immuun-overstimulatie
Dierexperimenteel onderzoek naar herinfectie is lastig omdat makaken beschermd zijn tegen herinfectie met SARS-CoV-2. De immunologie van deze en andere dieren is anders dan van de mens, zoals aangetoond bij de cytokinestorm veroorzaakt door TGN1412. De apen krijgen hier geen last van, terwijl deze sepsis bij mensen dodelijk is. Dit of een ander immunologisch mechanisme kan een rol spelen bij het verschil in de reactie op SARS-CoV-2 tussen mens en makaak. Het is evident dat dierproeven waarin de menselijke ziekte niet goed nagebootst kan worden geen goed voorspelmodel op kunnen leveren voor de mens. Vanuit de Federatie Medisch wetenschappelijke Verenigingen hielden we in 2016 een Federa-dag over gezonde wetenschap, meer waarde, minder afval. Of zoals sprekers zeiden: : slordige methodologie levert weinig waarde op voor patiënten.
Niet-steriele immuniteit
Klinisch gezien geven virussen twee soorten infecties: symptomatische en asymptomatische. Voor de epidemiologie zijn de infecties zonder klachten de gevaarlijkste omdat asymptomatische mensen ongeremd nieuwe contacten aangaan en andere kunnen besmetten. Na een infectie ontstaat meestal immuniteit tegen ziekte en vaak ook tegen infectie (steriele immuniteit). Immuniteit bij coronavirussen is kortdurend en doorgaans niet steriel. SARS-2 infecties zonder klachten komen veel voor en ook herinfectie kan asymptomatisch zijn. Bij SARS-2 infecties zien we echter dat mensen die niet ziek worden, heel lang virus blijven uitscheiden en dus anderen kunnen infecteren. Deze niet-steriele immuniteit kan een belangrijke bijdrage leveren aan de verspreiding van de epidemie. Mensen zonder klachten hebben immers geen reden om in quarantaine te gaan, tenzij ze via TTI worden opgespoord.
Hoe lang beschermt vaccinatie?
Dit is de grote onbekende en verschilt mogelijk per type vaccin en type immuniteit. De vele herinfecties suggereren dat de gemiddelde duur van immuniteit na infectie erg kort is (minder dan een jaar). De vaccinstudies kijken vooral naar de bescherming in de eerste paar maanden na vaccinatie omdat dit ongeveer de tijd is dat waarin ongeveer 1% van de deelnemers ziek wordt. Na een vooraf vastgesteld aantal ziektes bij proefpersonen wordt de codering doorbroken en het resultaat geanalyseerd. Het gevonden verschil tussen de vaccin- en controlegroep geeft de bescherming in die eerste paar maanden weer. Daarmee kan dus niet verteld worden of het vaccin over 6 of 12 maanden nog steeds immuniteit oplevert. Omdat onbekend is hoe immuniteit tegen SARS-2 werkt –welke antistoffen en/of cellulaire immuniteit zijn belangrijk? – is immuniteit ook moeilijk te meten. Als natuurlijke infecties maatgevend zijn voor de duur van immuniteit is het mogelijk dat mensen meermaals per jaar gevaccineerd moeten worden. De huidige inschatting is dat het echter een jaar duurt voordat iedereen eenmaal gevaccineerd is. We zijn nog niet zover dat we iedereen kunnen beschermen met vaccinatie.
Waartegen willen we beschermd zijn?
Pfizer en BioNTech juichten in een persbericht dat hun COVID-19 vaccin in ruim 90% van de gevallen effectief is. Gemiddeld dus goed tegen ziekte, in de geneeskunde is bekend dat een goed gemiddelde ook negatieve effecten bij sommige mensen kan betekenen. Minstens zo belangrijk is dat we niet met man en macht een vaccin ontwikkelen omdat mensen griepachtige klachten krijgen, maar vanwege sterfte en hoge morbiditeit in de vorm van blijvende ziekte. Geen van de zeven vaccinstudies bestudeert dit als primaire uitkomstmaat.
De invalshoek van het College ter Beoordeling van Geneesmiddelen (CBG) stelt mij teleur (Figuur 3). Objectief gezien maakt deze beoordeling een COVID-19 vaccin niet waardevoller dan een vaccin tegen verkoudheid. Een vaccin dat geen ernstige ziekte of sterfte voorkomt hoeft immers geen topprioriteit te hebben? Ik begrijp heel goed dat een COVID-19 vaccin in potentie meer zou kunnen, zoals het voorkomen van ernstige ziekte en sterfte. De huidige vaccinstudies hebben dat echter niet bewezen. Daarom zie ik hierin onvoldoende grond om heel Nederland te vaccineren, zonder dit eerst te bestuderen.
De invalshoek van het College ter Beoordeling van Geneesmiddelen (CBG) stelt mij teleur (Figuur 3). Objectief gezien maakt deze beoordeling een COVID-19 vaccin niet waardevoller dan een vaccin tegen verkoudheid. Een vaccin dat geen ernstige ziekte of sterfte voorkomt hoeft immers geen topprioriteit te hebben? Ik begrijp heel goed dat een COVID-19 vaccin in potentie meer zou kunnen, zoals het voorkomen van ernstige ziekte en sterfte. De huidige vaccinstudies hebben dat echter niet bewezen. Daarom zie ik hierin onvoldoende grond om heel Nederland te vaccineren, zonder dit eerst te bestuderen.
Figuur 3. CBG over gewenste effecten van vaccins.
Wie willen we beschermen?
Het vermoedelijke advies van de Gezondheidsraad en de EU bevat verschillende strategieën om groepen mensen met voorrang te beschermen. Oppervlakkig gezien lijken dit logische keuzes, maar het is gebouwd op het drijfzand van onbewezen en onuitgesproken aannames. Een wetenschappelijk advies zonder gezond boerenverstand vraagt om grondig te worden doorgespit.
Als tweede voorrangsgroep wordt vooral het zorgpersoneel genoemd. Persoonlijke bescherming tegen ziekte is fijn, maar heeft geen grote urgentie. Voorkomen van ernstige ziekte en sterfte wel, maar of de vaccins hier iets in doen is niet bewezen. Wat ook niet benoemd is, is het idee dat vaccinatie mogelijk zou voorkomen dat dat geïnfecteerde zorgmedewerkers kwetsbare mensen kunnen besmetten. Het is inderdaad zo dat immuniteit tegen de meeste virussen “steriel” is. Ik heb echter verschillende aanwijzingen gegeven dat SARS-2 immuniteit niet-steriel is. Als dat ook voor SARS-2 immuniteit na vaccinatie geldt, zijn gevaccineerde zorgmedewerkers wel zelf beschermd tegen ziekte, maar kunnen ze de kwetsbare zorgontvangers blijven besmetten. Dit zou onderzocht kunnen in standaard screening van gevaccineerd zorgpersoneel, iets wat ik eerder heb aanbevolen aan VWS.
De eerste groep zijn de kwetsbare mensen: 60-plussers en mensen met onderliggende ziekten. De motivatie hiervoor is helder: dit zijn mensen met een verhoogd risico om te sterven of ernstige gevolgen aan COVID-19 over te houden. Geen van de huidige vaccinstudies onderzoekt of ziekenhuis-, IC-opname en sterfte voorkomen kan worden. De afweer neemt af bij oudere mensen waardoor het niet onwaarschijnlijk is dat zij minder goed reageren op vaccinatie. Of oudere mensen beschermd worden na vaccinatie is ook nog niet onderzocht.
Als tweede voorrangsgroep wordt vooral het zorgpersoneel genoemd. Persoonlijke bescherming tegen ziekte is fijn, maar heeft geen grote urgentie. Voorkomen van ernstige ziekte en sterfte wel, maar of de vaccins hier iets in doen is niet bewezen. Wat ook niet benoemd is, is het idee dat vaccinatie mogelijk zou voorkomen dat dat geïnfecteerde zorgmedewerkers kwetsbare mensen kunnen besmetten. Het is inderdaad zo dat immuniteit tegen de meeste virussen “steriel” is. Ik heb echter verschillende aanwijzingen gegeven dat SARS-2 immuniteit niet-steriel is. Als dat ook voor SARS-2 immuniteit na vaccinatie geldt, zijn gevaccineerde zorgmedewerkers wel zelf beschermd tegen ziekte, maar kunnen ze de kwetsbare zorgontvangers blijven besmetten. Dit zou onderzocht kunnen in standaard screening van gevaccineerd zorgpersoneel, iets wat ik eerder heb aanbevolen aan VWS.
De eerste groep zijn de kwetsbare mensen: 60-plussers en mensen met onderliggende ziekten. De motivatie hiervoor is helder: dit zijn mensen met een verhoogd risico om te sterven of ernstige gevolgen aan COVID-19 over te houden. Geen van de huidige vaccinstudies onderzoekt of ziekenhuis-, IC-opname en sterfte voorkomen kan worden. De afweer neemt af bij oudere mensen waardoor het niet onwaarschijnlijk is dat zij minder goed reageren op vaccinatie. Of oudere mensen beschermd worden na vaccinatie is ook nog niet onderzocht.
Te waardevol om te verkwisten
De Nederlandse overheid lijkt te gaan voor de snelle inzet van COVID-19 vaccins met alle mogelijke risico’s van dien. Bij mijn weten zijn andere experts nog niet geraadpleegd voor een nieuwe versie van Lessons Learned. Een snelle inzet betekent in de praktijk nog een jaar. Uit mijn afwegingen blijkt dat de vaccins mogelijk nuttig kunnen zijn in de strijd tegen COVID-19, maar dat er te veel onbekendheden zijn met betrekking tot de veiligheid van vaccins. Als een vaccin een verkeerde afweerrespons veroorzaakt, kan het zelfs zorgen voor een slechtere afweer tegen de pathogeen. De European Medicines Agency (EMA) heeft aangedrongen om zoveel mogelijk mensen uit risicogroepen mee te nemen in studies (Figuur 4). Een percentage van deze mensen zal ernstig ziek worden na COVID-19 infectie. De huidige vaccinstudies zijn statistisch underpowered voor deze analyse, dus geven waarschijnlijk geen antwoord of vaccinatie de ziekte verminderd of verergerd. Methodologisch is deze aanpak ondermaats en biedt onvoldoende bescherming om mensenlevens te beschermen.
Wat is een betere aanpak? De Federa-dag in 2017 ging over experimenten op mens en dier: te waardevol om te verkwisten. Belangrijk is dat de relevante doelgroepen in de studies zitten. Hart- en vaatziekten zijn een belangrijke onderliggende risicofactor voor sterfte aan COVID-19. Daar blijkt leeftijd een grote invloed te hebben op het risico. Leeftijd zou dit dus ook kunnen hebben in de COVID-19 vaccin studies en dus moet het worden geïncludeerd. Zonder zorgvuldig gecontroleerd onderzoek op mensen is iedereen proefkonijn. Immunologisch onderzoek naar probiotica liet al eerder zien dat het effect bij milde ziekte positief was, maar negatief bij een andere ernstigere infectie.
Moeten we dan een jaar wachten, zoals de CBG vreest (Figuur 3)? Nee, de logische vervolgstap zou zijn om de aangeschafte vaccins te gebruiken voor een geblindeerde en gerandomiseerde fase 3 studie bij de kwetsbare mensen. De primaire uitkomstmaat van die studie is de ernstige morbiditeit (ziekenhuis- en IC-opname) en sterfte onder deze groep. In deze groep zullen in de derde coronagolf, die ongetwijfeld komt voordat Nederland voldoende vaccins heeft om iedereen te injecteren, voldoende ernstige COVID-19 gevallen zijn om te zien of het vaccin een positief of negatief effectief heeft. Zodra de uitkomst van dit gezondheidsrisico in de kwetsbare populatie bekend is, kan worden besloten om andere kwetsbare mensen juist wel of juist niet dit vaccin te geven. In geval dat het niet of averechts werkt, is slechts een kleine groep gevaccineerd. Als het vaccin wel beschermt, kan iedereen worden gevaccineerd inclusief de mensen die niet tijdens de studie waren gevaccineerd (de controles). Zo worden mensen maximaal beschermd volgens het beste aanwezige medische bewijs, en wordt voorkomen dat verkeerde aannames leiden tot een drastische verkwisting van mensenlevens. Zoals ik de beide Federa-dagen mocht samenvatten: mensenlevens zijn te kostbaar om te verkwisten met slordige wetenschap.
Wat is een betere aanpak? De Federa-dag in 2017 ging over experimenten op mens en dier: te waardevol om te verkwisten. Belangrijk is dat de relevante doelgroepen in de studies zitten. Hart- en vaatziekten zijn een belangrijke onderliggende risicofactor voor sterfte aan COVID-19. Daar blijkt leeftijd een grote invloed te hebben op het risico. Leeftijd zou dit dus ook kunnen hebben in de COVID-19 vaccin studies en dus moet het worden geïncludeerd. Zonder zorgvuldig gecontroleerd onderzoek op mensen is iedereen proefkonijn. Immunologisch onderzoek naar probiotica liet al eerder zien dat het effect bij milde ziekte positief was, maar negatief bij een andere ernstigere infectie.
Moeten we dan een jaar wachten, zoals de CBG vreest (Figuur 3)? Nee, de logische vervolgstap zou zijn om de aangeschafte vaccins te gebruiken voor een geblindeerde en gerandomiseerde fase 3 studie bij de kwetsbare mensen. De primaire uitkomstmaat van die studie is de ernstige morbiditeit (ziekenhuis- en IC-opname) en sterfte onder deze groep. In deze groep zullen in de derde coronagolf, die ongetwijfeld komt voordat Nederland voldoende vaccins heeft om iedereen te injecteren, voldoende ernstige COVID-19 gevallen zijn om te zien of het vaccin een positief of negatief effectief heeft. Zodra de uitkomst van dit gezondheidsrisico in de kwetsbare populatie bekend is, kan worden besloten om andere kwetsbare mensen juist wel of juist niet dit vaccin te geven. In geval dat het niet of averechts werkt, is slechts een kleine groep gevaccineerd. Als het vaccin wel beschermt, kan iedereen worden gevaccineerd inclusief de mensen die niet tijdens de studie waren gevaccineerd (de controles). Zo worden mensen maximaal beschermd volgens het beste aanwezige medische bewijs, en wordt voorkomen dat verkeerde aannames leiden tot een drastische verkwisting van mensenlevens. Zoals ik de beide Federa-dagen mocht samenvatten: mensenlevens zijn te kostbaar om te verkwisten met slordige wetenschap.
Figuur 4. CBG over het EMA advies voor vaccinstudies