Palet aan testenJohn Jacobs, 12 september 2020 |
Testen is cruciaal in de virologie. Virologen hebben een breed scala aan testen om aan te tonen dat iemand geïnfecteerd is met SARS-2, de oorzaak van COVID-19. Het is belangrijk om onderscheid te maken tussen de verschillende testen want ze tonen andere zaken aan. Sommige testen tonen het virus aan, andere dat iemand geïnfecteerd of ziek is (geweest). Veel testen zijn oorspronkelijk gemaakt in de klinische setting. Epidemiologisch onderzoek stelt deels andere eisen aan testen.
Aantonen virus
Directe testen tonen het virus of onderdelen van het virus aan. Het voordeel van dit soort testen is dat ze de actuele situatie vaststellen en een maat kunnen geven voor de hoeveelheid virus.
Viruskweek voor infectieus virus
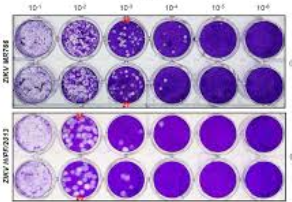
De klassieke gouden standaard voorbeeld is de viruskweek die infectieus virus aantoont. Door een verdunningsreeks te maken van het aantal plaque vormende eenheden kan de virusconcentratie worden berekend (Figuur 1). Het nadeel is dat de test meerdere dagen duurt en in een BSL-3 lab moet worden uitgevoerd. Dat is een hoger veiligheidsniveau dan het gebruikelijk BSL-2 lab en dus niet overal beschikbaar. Ook is de test moeilijk opschaalbaar.
Figuur 1. Verdunningsreeks van een virus plaque titratie. In de witte gebieden zijn cellen gedood door het virus. De cijfers boven de reeks geven de verdunning weer. Twee verschillende samples zijn in duplo weergegeven
RT-qPCR voor virus RNA
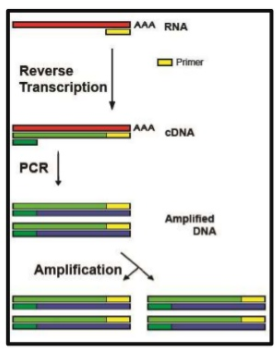
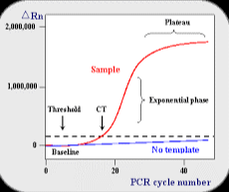
De meest gebruikte test en de nieuwe gouden standaard om virus RNA aan te tonen is RT-PCR (Figuur 2). RNA is chemisch en biologisch instabiel, dus als het infectieuze virus weg is, is het RNA ook verdwenen.** RT-PCRis ook de meest gevoelige test, want het gros van de geproduceerde virussen is niet infectieus - als het RNA bevat kan het worden aangetoond met RT-PCR. Technisch bestaat deze test uit een aantal stappen: (i) RNA isolatie, (ii) Reverse Transcriptie (RT) van RNA naar cDNA, (iii) PCR amplificatie van cDNA. Door (iv) het amplificatieproduct real-time te meten krijgt de test een kwantitatieve (q) uitslag (RT-qPCR). Deze test duurt ongeveer 3 uur. Veel andere moleculair biologische technieken lijken hierop, maar zijn vaak net iets sneller (1,5 uur).
Figuur 2. Links RT-PCR van virus RNA, met daarnaast kwantificatie door middel van Cycle threshold (Ct) nummer. Hoe vaker het DNA vermenigvuldigd moet worden, hoe minder virus RNA er in het sample zat, dus hoe hoger de Ct hoe minder virus er in een monster zat.
Sandwich ELISA voor virusantigeen
Voor het aantonen van viruseiwitten zijn er verschillende technieken met antistoffen of moleculaire identificatie.
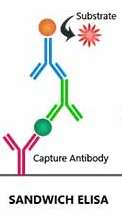
In de sandwich ELISA voor viruseiwitten zijn reageervaatjes gecoat met antistoffen tegen SARS-2. Het monster wordt in deze vaatjes gelaten en na incubatie weer weggewassen. Vervolgens wordt met een tweede (en soms derde) antilichaam de aanwezigheid van het virus aangetoond (Figuur 3). Het aantal stappen in deze test maakt dat deze meerdere uren duurt. Biosensoren met antistoffen kunnen een dergelijke test sneller uitvoeren (Qiu), maar die apparaten zijn vrij duur.
In de sandwich ELISA voor viruseiwitten zijn reageervaatjes gecoat met antistoffen tegen SARS-2. Het monster wordt in deze vaatjes gelaten en na incubatie weer weggewassen. Vervolgens wordt met een tweede (en soms derde) antilichaam de aanwezigheid van het virus aangetoond (Figuur 3). Het aantal stappen in deze test maakt dat deze meerdere uren duurt. Biosensoren met antistoffen kunnen een dergelijke test sneller uitvoeren (Qiu), maar die apparaten zijn vrij duur.
Figuur 3. Sandwich ELISA. Antistof gecoate reageervaatjes vangen het virus op uit het sample. Vervolgens worden andere antistoffen toegevoegd om een gebonden virus aan te tonen
Massaspectrometrie voor viruseiwit
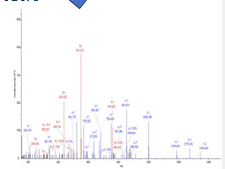
Bij massaspectrometrie van viruseiwitten worden de eiwitten eerst in stukken gehakt door zuur en/of enzymen (Nikolaev). Die eiwitfragmenten worden vervolgens gedetecteerd en verder gekarakteriseerd op welke aminozuren in een eiwit zitten. Dat maakt ook deze test zeer specifiek. Omdat de virus fragmentatie stappen sterk verkort kunnen worden kan deze test versneld worden tot ½ a 1 uur (Figuur 4). Groot nadeel is dat de massaspectrometer een duur en geavanceerde apparaat is.
Figuur 4. Massaspectrometrie. Pieken correleren met specifieke molecuulgroottes die herleid kunnen worden naar de aminozuren van viruseiwitten
Sampling
Alle testen die het virus direct aantonen zijn afhankelijk van de methode van bemonsteren (sampling). De normale procedure is dat de neusholte en/of mond-holte (de keel) bemonsterd wordt. Echter het virus blijft niet op deze locaties (NYTimes), maar migreert naar de longen en later naar de bloedcirculatie (Jacobs, zie ook). Als het virus niet meer in de neus- en/of keelholte is kan iemand nog wel longontsteking en systemische infectie hebben, maar is het virus niet aan te tonen waar bemonsterd wordt. Dat kan leiden tot een negatief testresultaat.
Specifieke immuunreacties
Een heel andere strategie is het aantonen van de afweerreactie tegen een virus. Zowel antistoffen als antigeen-specifieke T-cellen kunnen wijzen op een huidige, recente of eerder doorgemaakte infectie. Specifiek T-cellen aantonen vraagt een specialistisch lab en is complex.
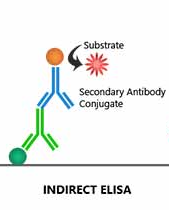
Antistoffen zijn met een indirecte ELISA goed aan te tonen (Figuur 5). Het reageervaatje wordt dan gecoat met viruseiwitten waarna antistoffen hiertegen kunnen binden. Met antistoffen tegen de antistoffen in het monster kan worden aangetoond of iemand antistoffen heeft, en welk type (IgM, IgG).
Antistoffen zijn met een indirecte ELISA goed aan te tonen (Figuur 5). Het reageervaatje wordt dan gecoat met viruseiwitten waarna antistoffen hiertegen kunnen binden. Met antistoffen tegen de antistoffen in het monster kan worden aangetoond of iemand antistoffen heeft, en welk type (IgM, IgG).
Figuur 5. Indirecte ELISA. Buisjes zijn gecoat met virus. Antistoffen in het sample kunnen hieraan binden. Vervolgens worden die antistoffen gedetecteerd met anti-antistof-antistoffen.
Afweer reactie
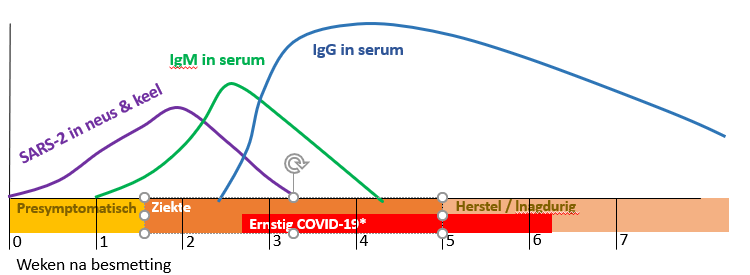
Antistoffen tonen niet aan of iemand geïnfecteerd is, maar geven informatie over de afweerreactie tegen het virus (Figuur 6). Ook vaccins kunnen antistoffen induceren. De belangrijkste antistoffen zijn immunoglobuline M (IgM) en IgG. IgM wordt als eerste in de infectie gemaakt en later vervangen door IgG dat specifieker is (Figuur 5). Met antistoffen tegen deze antistoffen kan worden aangetoond welk type antistoffen iemand heeft. Een ELISA duurt enkele uren.
Figuur 6. Verloop infectie, ziekte en antistoffen (IgM en IgG) tegen SARS-2. De ziekte begint presymptomatisch waarna een deel van de mensen klachten krijgt en ziek wordt. Sommigen krijgen later ernstig COVID-19. De herstel periode kan kort zijn, maar duurt bij een minderheid langer dan 3 of zelfs 6 maanden.
Kruisreactiviteit
SARS-2 behoort tot de groep coronavirussen, waarin verkoudheidsvirussen vergelijkbare eiwitten hebben voor processen in het virus (niet aan de buitenkant). De indirecte ELISA is een test om antistoffen tegen het virus te meten (Figuur 6). Hoewel antistoffen zeer specifiek zijn voor een eiwitdomein, kunnen sommige antistoffen kruisreageren met eiwitten van andere coronavirussen. In de testopzet kan gekozen worden om die eiwitten juist wel of juist niet mee te nemen, afhankelijk van de vraagstelling.
Ziekteverschijnselen
Aantonen symptomen
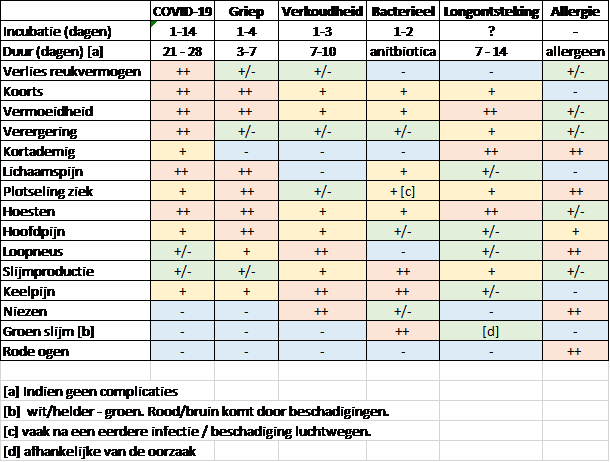
Behalve de viruskweek zijn alle bovenstaande technieken de laatste 50 jaar nieuw ontwikkeld. Virussen aantonen kostte in het verleden veel tijd en meestal beperkte men zich tot zieke personen aantonen. Bij TTI heb ik geschreven dat dit niet optimaal is voor de bestrijding van epidemieën, omdat niet elke infectie symptomen oplevert. Mensen die wel symptomen hebben van COVID-19 hebben grieperige klachten (Figuur 7). De meest specifieke klacht is verlies van het reukvermogen. Indien iemand het reukvermogen verloren heeft door een infectie, zonder buitensporig veel slijm, dan is de diagnose COVID-19 vrijwel zeker. Maar niet iedereen heeft alle klachten. Asymptomatische klachten en aspecifieke klachten zijn de redenen waarom veel gevallen van COVID-19 gemist worden. Als infecties niet geïdentificeerd worden, kan het virus zich blijven verspreiden.
Figuur 7. Symptomen van enkele luchtweginfecties
Doel van testen
Kliniek versus epidemie bestrijding
Het belangrijkste in de ziekenhuis diagnostiek is zorgvuldigheid en de aanvullende medische kennis. Testen voor TTI dienen snel te bepalen wie mogelijk infectieus is en wie niet (Mina). Slim testbeleid binnen bron- en contactonderzoek minimaliseert de kans op vals-positieven. Voor diagnostiek is de aanpak volledige anders. De diagnostische testen voor SARS-2 vragen (a) meer tijd, (b) meer specialistisch personeel en/of (c) meer specialistische apparatuur dan ideaal is voor een snelle test die men massaal wilt uitvoeren voor TTI. Een screening met een sneltest kan bepalen wie wel of niet getest moet worden.
Twee testen
Sneltest
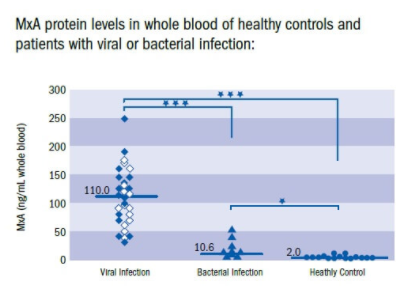
Veel testcapaciteit wordt gebruikt door gezonde mensen, waar infectie met een sneltest uitgesloten kan worden. Sneltesten zijn ontwikkeld voor diagnostiek van infecties, maar niet specifiek voor het aantonen van SARS-2. Ze tonen bijvoorbeeld aan of iemand een virusinfectie heeft. De logica is dat iedereen met een SARS-2 infectie een virusinfectie heeft, maar iemand met een virusinfectie kan ook een gewone verkoudheid of griep hebben. Een sneltest kan binnen 10 minuten aantonen of iemand een virusinfectie heeft (Shirley). De test toont het eiwit Myxovirus resistance A (MxA) aan dat alleen door type I interferon wordt aangemaakt. Type I interferon is specifiek voor virusinfecties. Mensen die positief scoren op een virusinfectie zouden dan vervolgens getest kunnen worden op SARS-2. Dat vermindert het aantal benodigde testen en werkt daardoor veel sneller.
Figuur 8. MxA test voor aantonen virusinfectie
Bevestiging SARS-2
Een snelle screening op virus en bacterie infecties zou een goede aanvulling zijn op de veiligheid bij gelegenheden waar veel mensen samenkomen, zoals voetbalwedstrijden, concerten, voorstellingen en volksfeesten. Sommigen denken zelfs aan een sneltest om elke dag thuis te uitvoeren (nytimes) met het gemak van een zwangerschapstest. Na een snelle test voor virusinfectie is, bij een positieve uitslag, nog een test nodig om aan te tonen dat het SARS-2 is en niet influenza of een verkoudheidsvirus.
Vals-positief en vals-negatief *
Geen enkele test is perfect. Elke test mist een aantal besmette gevallen (vals-negatief) en wijst ten onrechte mensen aan als besmet (vals-positief). Hoe erg dat is hangt in de praktijk af van hoe goed de test is, hoeveel besmettingen in de populatie zitten en de teststrategie.
Hoe goed de test is wordt aangegeven met specificiteit en sensitiviteit. Specificiteit is 1 - de kans dat een negatief persoon positief getest wordt. Dus als virusvrij persoon 1% kans heeft om positief uit de test te komen, dan is specificiteit 100%-1% = 99%.
Sensitiviteit is de gevoeligheid van de test om het virus aan te tonen in een geïnfecteerd persoon. Als 95% van de infecties kan worden aangetoond dan is de sensitiviteit 95%.
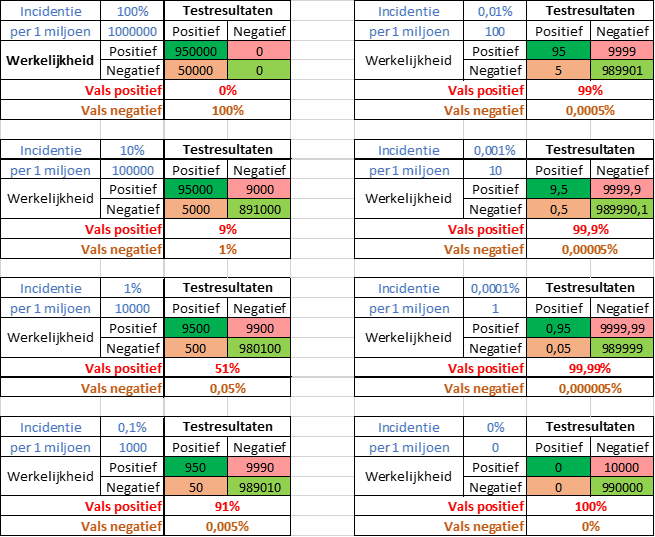
Incidentie is hoeveel het virus voorkomt in de populatie, dus hoeveel procent van de mensen besmet is. Figuur 9 laat zien dat de test met een specificiteit van 99% en een sensitiviteit van 95%. Vals-negatieve resultaten kunnen alleen worden verkregen binnen de mensen die positief zijn, en omgekeerd vals-positief alleen als mensen negatief zijn. Virusinfecties hebben vaak een lage incidentie in de bevolking. 1 op de 1000 (0,1%) linksonder wordt gezien als erg hoog. In dit voorbeeld zou dan 91% van de test vals-positief zijn. Als de incidentie nog een factor 10 lager ligt (rechtsboven) zelfs 99%.
Hoe goed de test is wordt aangegeven met specificiteit en sensitiviteit. Specificiteit is 1 - de kans dat een negatief persoon positief getest wordt. Dus als virusvrij persoon 1% kans heeft om positief uit de test te komen, dan is specificiteit 100%-1% = 99%.
Sensitiviteit is de gevoeligheid van de test om het virus aan te tonen in een geïnfecteerd persoon. Als 95% van de infecties kan worden aangetoond dan is de sensitiviteit 95%.
Incidentie is hoeveel het virus voorkomt in de populatie, dus hoeveel procent van de mensen besmet is. Figuur 9 laat zien dat de test met een specificiteit van 99% en een sensitiviteit van 95%. Vals-negatieve resultaten kunnen alleen worden verkregen binnen de mensen die positief zijn, en omgekeerd vals-positief alleen als mensen negatief zijn. Virusinfecties hebben vaak een lage incidentie in de bevolking. 1 op de 1000 (0,1%) linksonder wordt gezien als erg hoog. In dit voorbeeld zou dan 91% van de test vals-positief zijn. Als de incidentie nog een factor 10 lager ligt (rechtsboven) zelfs 99%.
Figuur 9. Effect van incidentie op percentage vals-positieve en vals-negatieve testresultaten. Voorbeeld voor test met 99% specificiteit, 95% sensitiviteit en verschillende incidentie (aangegeven in blauw als % en aantal per 1 miljoen).
Combinatie van testen voor betrouwbaarder resultaat *
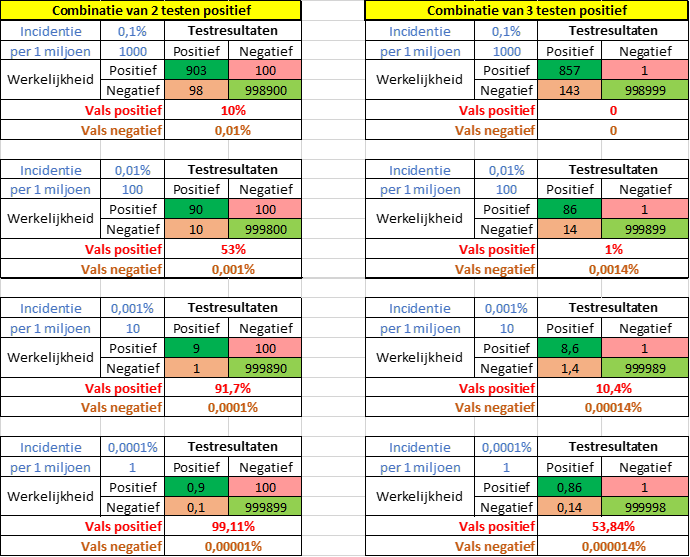
Aangezien virussen vaak een erg lage incidentie in de bevolking hebben wordt het percentage vals-positieve resultaten erg snel erg hoog. Daarom combineren labs vaak meerdere labtesten, zoals RT-PCR's op verschillende eiwitten. Als twee testen met een specificiteit van 99% worden gecombineerd (beide moeten positief zijn), wordt de nieuwe specificiteit 99,99%. Dit gaat ten koste van de sensitiviteit, die daalt naar 90%). Het percentage vals-positieven daalt dan sterk (Figuur 10). Nog extremer wordt het bij drie testen: 99,9999% specificiteit en 86% sensitiviteit. Vrijwel alle labs die diagnostische RT-qPCR uitvoeren doen 2 of 3 verschillende testen.
Figuur 10. Effect van incidentie op percentage vals-positieve en vals-negatieve testresultaten bij 2 of 3 testen met elke 99% specificiteit, 95% sensitiviteit en verschillende incidentie (aangegeven in blauw als % en aantal per 1 miljoen).
John Jacobs
12 september 2020
Secties met * zijn 26 september toegevoegd. Zin met ** is 13 oktober aangevuld
12 september 2020
Secties met * zijn 26 september toegevoegd. Zin met ** is 13 oktober aangevuld