COVID-19
ImmuunreactiesJohn Jacobs, 28 november 2020. |
Twee componenten
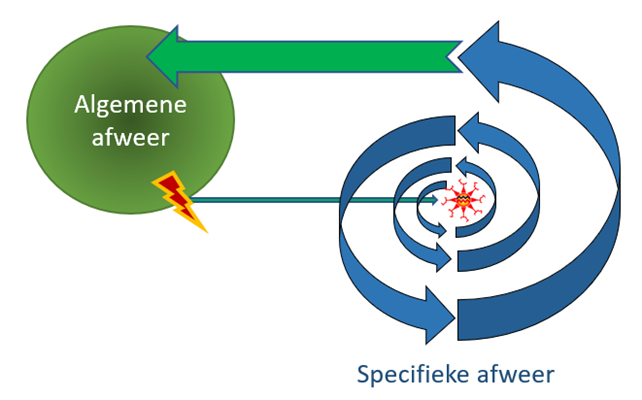
Ons afweersysteem bestaat uit twee componenten die goed samenwerken: de algemene (natuurlijke) afweer en de specifieke afweer (Figuur 2). Beide componenten gebruiken duizenden variaties van honderden moleculen die onderling vaak een beetje verschillen. Deze moleculen kunnen markers zijn op cellen (CD-antigenen), eiwitten in cellen, communicatie eiwitten tussen cellen (cytokines) of eiwitten die afweerfuncties uitvoeren (celdodende eiwitten, complement en stollingseiwitten). Door de talloze kleine verschillen kan het afweersysteem heel subtiel zaken regelen. Ook hebben kleine genetische foutjes, zoals het missen van een bepaald gen, bij de meeste ziektes weinig invloed omdat een groot deel van de functie door een ander molecuul wordt overgenomen. Mensen die interferon beta missen zijn extreem gevoelig voor enkele ernstige virusinfecties zoals COVID-19. De sterkte van natuurlijke afweer is vooral afhankelijk van iemands voeding, conditie, leeftijd en leefstijl. Vitamine D en interferon-beta zijn belangrijke factoren voor een gezonde natuurlijke afweer.
Natuurlijke afweer herkent en bestrijdt gevaar voor het lichaam. Gevaar kan zijn een bekende gevaarlijke structuur zoals een virus, maar ook celdood. Bij gevaar worden de antigenen uit het weefsel meegenomen en aangeboden aan het specifieke afweersysteem.
Natuurlijke afweer herkent en bestrijdt gevaar voor het lichaam. Gevaar kan zijn een bekende gevaarlijke structuur zoals een virus, maar ook celdood. Bij gevaar worden de antigenen uit het weefsel meegenomen en aangeboden aan het specifieke afweersysteem.
Figuur 1. Algemene en specifieke afweer
(1) De natuurlijke afweer herkent gevaar, zoals celdood of een structuur van een ziekteverwekker, zoals dsRNA. (2) Dendritische cellen presenteren antigen aan de specifieke afweer (B, Tc en Th cellen, zie Figuur 4). (3) De specifieke afweer vermenigvuldigt zich door celdeling tot een sterke, specifieke afweerreactie. (4) De specifieke afweer dirigeert afweerreacties tegen ziekteverwekkers door specifieke en natuurlijke afweer.
(1) De natuurlijke afweer herkent gevaar, zoals celdood of een structuur van een ziekteverwekker, zoals dsRNA. (2) Dendritische cellen presenteren antigen aan de specifieke afweer (B, Tc en Th cellen, zie Figuur 4). (3) De specifieke afweer vermenigvuldigt zich door celdeling tot een sterke, specifieke afweerreactie. (4) De specifieke afweer dirigeert afweerreacties tegen ziekteverwekkers door specifieke en natuurlijke afweer.
Virus-specifieke afweer
De kracht van de specifieke afweer is dat die kleine structuren (vaak eiwitten) van een ziekteverwekker herkent en daar een geheugen voor krijgt, waardoor afweer nog effectiever is. Als deze afweer voorkomt dat mensen ziek worden noemen we dit immuniteit. Als de afweer ook infectie voorkomt noemen we dit steriliserende immuniteit. Infectie wil zeggen dat het virus zich vermenigvuldigt in de mens. De biologie schakelt een evolutionair ontwerpprincipe in om verschillende moleculen voor herkenning te maken. Virus-specifieke afweer kunnen antistoffen gemaakt door B-cellen zijn of cellulaire afweer van cytotoxische T-cellen (Tc).
Een virusinfectie leidt tot productie van viruseiwitten in de cel en vrij virus buiten de cel (Figuur 3). Eiwitproductie in een cel is nodig om cytotoxische (celdodende) T (Tc) cellen te krijgen. Deze Tc doden geïnfecteerde cellen (cellulaire immuniteit), maar zijn niet effectief tegen vrij virus.
B-cellen maken antistoffen binden die kunnen binden aan vrij virus. Antistoffen komen niet in de cel, maar kunnen vrij virus neutraliseren. Virus met antistoffen is lastiger te kweken en zal waarschijnlijk minder snel andere mensen infecteren. Het is niet bewezen dat antistoffen beschermen tegen ziekte, immers mensen die ernstig ziek zijn hebben de hoogste titers aan neutraliserende antistoffen.
Een virusinfectie leidt tot productie van viruseiwitten in de cel en vrij virus buiten de cel (Figuur 3). Eiwitproductie in een cel is nodig om cytotoxische (celdodende) T (Tc) cellen te krijgen. Deze Tc doden geïnfecteerde cellen (cellulaire immuniteit), maar zijn niet effectief tegen vrij virus.
B-cellen maken antistoffen binden die kunnen binden aan vrij virus. Antistoffen komen niet in de cel, maar kunnen vrij virus neutraliseren. Virus met antistoffen is lastiger te kweken en zal waarschijnlijk minder snel andere mensen infecteren. Het is niet bewezen dat antistoffen beschermen tegen ziekte, immers mensen die ernstig ziek zijn hebben de hoogste titers aan neutraliserende antistoffen.
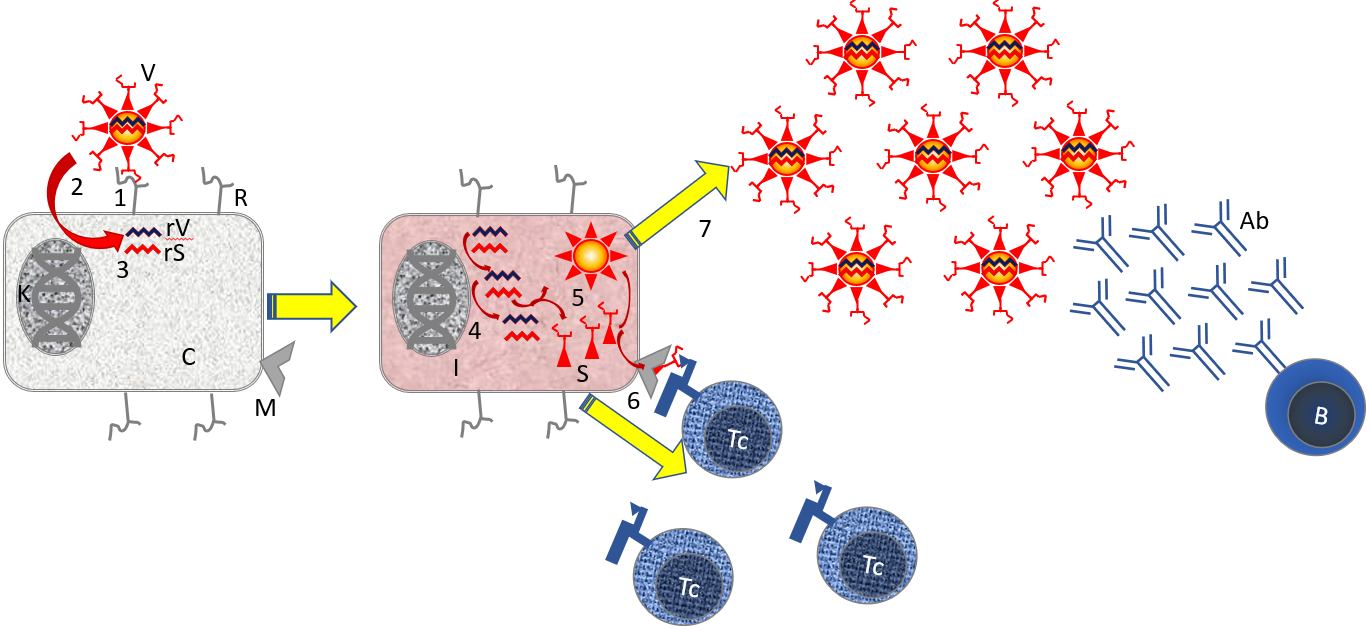
Figuur 3 Virusinfectie en afweer.
Onderdelen: [B] B-cel; [C} cytoplasma van cel; [I] cytoplasma van geïnfecteerde cel. [K] Kern met DNA; [R] ACE-2 Receptor; [rS] Virus RNA coderend voor Spike eiwit; [rV] Virus RNA coderend voor cellulaire genen; [S] Virus Spike eiwit dat bindt aan de ACE-2 Receptor voor infectie. [Tc] cytotoxische T cel; [V] virus.
Stapsgewijs mechanisme: [1] Het SARS-2 virus bindt aan de ACE-2-Receptor op de cel. [2] Receptor-binding induceert membraanfusie en het virus komt in het cytoplasma van de cel. [3] Het virus ontmantelt zich het virale RNA komt in de cel. Dit RNA bevat functies die de cel aanzetten tot virusreplicatie, die viruseiwitten produceren en die het afweersysteem beïnvloeden. [4] Het virale RNA wordt vermenigvuldigd in de cel door het virus RNA-polymerase. [5] Door het vertalen van het virus mRNA worden in de cel virus eiwitten gemaakt. [6] Kleine stukjes viruseiwitten (peptiden) worden in de context van MHC I gepresenteerd aan cytotoxische T-cellen [Tc]. [7] vrij virus wordt geproduceerd, waartegen B-cellen antistoffen maken.
Niet getekend: Stappen 6 + 7 worden ondersteund doordat specialistische afweercellen (dendritische cellen; DC) Kleine stukjes viruseiwitten in de context van MHC-II presenteren aan helper T-cellen [Th]. Zie afbeelding 5 in Veiligheid voor de huid zonder dierenleed.
Onderdelen: [B] B-cel; [C} cytoplasma van cel; [I] cytoplasma van geïnfecteerde cel. [K] Kern met DNA; [R] ACE-2 Receptor; [rS] Virus RNA coderend voor Spike eiwit; [rV] Virus RNA coderend voor cellulaire genen; [S] Virus Spike eiwit dat bindt aan de ACE-2 Receptor voor infectie. [Tc] cytotoxische T cel; [V] virus.
Stapsgewijs mechanisme: [1] Het SARS-2 virus bindt aan de ACE-2-Receptor op de cel. [2] Receptor-binding induceert membraanfusie en het virus komt in het cytoplasma van de cel. [3] Het virus ontmantelt zich het virale RNA komt in de cel. Dit RNA bevat functies die de cel aanzetten tot virusreplicatie, die viruseiwitten produceren en die het afweersysteem beïnvloeden. [4] Het virale RNA wordt vermenigvuldigd in de cel door het virus RNA-polymerase. [5] Door het vertalen van het virus mRNA worden in de cel virus eiwitten gemaakt. [6] Kleine stukjes viruseiwitten (peptiden) worden in de context van MHC I gepresenteerd aan cytotoxische T-cellen [Tc]. [7] vrij virus wordt geproduceerd, waartegen B-cellen antistoffen maken.
Niet getekend: Stappen 6 + 7 worden ondersteund doordat specialistische afweercellen (dendritische cellen; DC) Kleine stukjes viruseiwitten in de context van MHC-II presenteren aan helper T-cellen [Th]. Zie afbeelding 5 in Veiligheid voor de huid zonder dierenleed.
Specialisatie van afweer
Verschillende vormen van afweer worden gecoördineerd door verschillende soorten helper T-cellen (Th). Deze houden het afweersysteem bij de eerder gemaakte keuze en versterken deze (Figuur 1). Meestal is dat een voordeel, omdat het lichaam ziekteverwekkers, nadat ze ooit schade hebben aangericht, efficiënt op de juiste manier wil opruimen. Soms is het echter een nadeel, zoals bij mensen die allergisch zijn geworden die na herhaald blootstellen steeds sterker reageren met de beruchte anafylactische shock als mogelijk gevolg. Bij extreme afweerreacties, zoals een shock kan het immuunsysteem ineens omslaan naar actieve bescherming door tolerantie om te proberen te voorkomen dat het eigen afweersysteem de mens doodt.
De algemene gedachte is dat antistoffen belangrijker zijn in de afweer tegen bacteriën en dat cellulaire afweer belangrijker is tegen virussen, omdat dit de cellen die virussen maken bestrijdt. Dit is echter een complex gebied van de immunologie waar veel visies en uitzonderingen op zijn, niet in de laatste plaats door de vele ontsnappingsstrategieën van virussen.
Bovenstaand is belangrijk om te realiseren in de virusimmuunziekte die COVID-19 is. Keuzes in de vroege afweer, zoals door een vaccin of een eerdere infectie, kunnen grote invloed hebben op de afweer bij een latere infectie.
De algemene gedachte is dat antistoffen belangrijker zijn in de afweer tegen bacteriën en dat cellulaire afweer belangrijker is tegen virussen, omdat dit de cellen die virussen maken bestrijdt. Dit is echter een complex gebied van de immunologie waar veel visies en uitzonderingen op zijn, niet in de laatste plaats door de vele ontsnappingsstrategieën van virussen.
Bovenstaand is belangrijk om te realiseren in de virusimmuunziekte die COVID-19 is. Keuzes in de vroege afweer, zoals door een vaccin of een eerdere infectie, kunnen grote invloed hebben op de afweer bij een latere infectie.
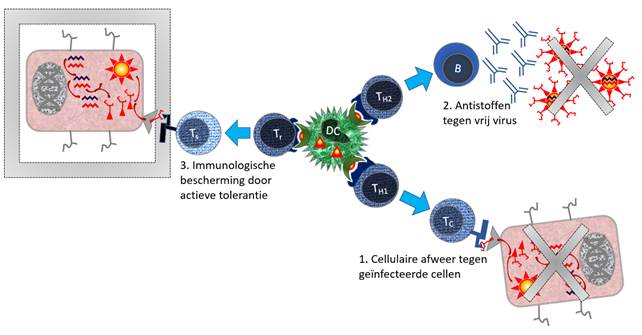
Figuur 4. Afstemming afweerreacties door T-Helper cellen.
Zie ook Figuur 3. Verdere onderdelen: [B] B-cel; [DC] Dendritische cel; [Tc} cytotoxische T cel; [Th1] T-helper type 1; [Th2] T-helper type 2; [Tr] Regulator T cel (Th-achtige cel die tolerantie bevordert). [Ts] Suppressor T cel, Tc-achtige cel die actief het weefsel beschermt tegen afweerreacties.
Stapsgewijs mechanisme: Dendritische cellen presenteren antigeen in MHC-II [1] Bij presentatie aan T-helper type 1 cellen zullen deze cytotoxische T-cellen stimuleren. Cytotoxische T-cellen doden virus-geïnfecteerde cellen. [2] Bij presentatie aan T-helper type 2 cellen zullen deze B-cellen stimuleren tot antistofproductie. Antistoffen zijn efficiënt in het opruimen van vrij virus. [3] Bij presentatie aan regulator T cellen zullen deze antigeen-specifieke tolerantie stimuleren. Deze cellen beschermen weefsel actief. Dit is belangrijk om te voorkomen dat het afweersysteem eigen gezond weefsel afstoot. Binnen elke route zijn talloze subtiele variaties.
Zie ook Figuur 3. Verdere onderdelen: [B] B-cel; [DC] Dendritische cel; [Tc} cytotoxische T cel; [Th1] T-helper type 1; [Th2] T-helper type 2; [Tr] Regulator T cel (Th-achtige cel die tolerantie bevordert). [Ts] Suppressor T cel, Tc-achtige cel die actief het weefsel beschermt tegen afweerreacties.
Stapsgewijs mechanisme: Dendritische cellen presenteren antigeen in MHC-II [1] Bij presentatie aan T-helper type 1 cellen zullen deze cytotoxische T-cellen stimuleren. Cytotoxische T-cellen doden virus-geïnfecteerde cellen. [2] Bij presentatie aan T-helper type 2 cellen zullen deze B-cellen stimuleren tot antistofproductie. Antistoffen zijn efficiënt in het opruimen van vrij virus. [3] Bij presentatie aan regulator T cellen zullen deze antigeen-specifieke tolerantie stimuleren. Deze cellen beschermen weefsel actief. Dit is belangrijk om te voorkomen dat het afweersysteem eigen gezond weefsel afstoot. Binnen elke route zijn talloze subtiele variaties.
Andere immuniteit
Coronavirussen hebben een opmerkelijke relatie met het afweersysteem. Net als bij verkoudheidsvirussen, zien we bij SARS-2 dat de afweerreactie ziek maakt, alleen is de ziekte door SARS-2 veel ernstiger. Bij luchtwegvirussen (influenza (griep), coronavirussen, RSV en rhinovirussen) leidt immuniteit tegen de ziekte niet tot immuniteit tegen het virus. Mensen die immuun zijn kunnen gewoon andere besmetten, hetgeen grote gevolgen heeft voor het principe van groepsimmuniteit.
Een aantal eiwitten in coronavirussen hebben overeenkomsten met eiwitten in andere coronavirussen, zoals verkoudheidsvirussen. Afweerreacties hiertegen kunnen leiden tot kruisimmuniteit door antistoffen of cellulaire afweer. Dit is een mogelijk verklaring waarom kinderen, die vaak verkouden zijn, minder vaak ziek worden van SARS-2. Opvallend, kinderen hebben zelden antistoffen tegen SARS-2. Het Spike eiwit dat in de vaccins gebruikt wordt, verschilt zo sterk tussen coronavirussen dat hier geen kruisimmuniteit te verwachten is.
De sterkste afweerreactie is tegen het Spike eiwit. Na infectie zijn mensen slechts korte tijd immuun tegen corona verkoudheidsvirussen en kunnen binnen opnieuw ziek worden van hetzelfde virus. Mogelijk verspreiden neutraliserende antistoffen het virus door het lichaam. Bij een SARS-1 werd verergering van longziekte gezien na blootstelling met virus.
Een aantal eiwitten in coronavirussen hebben overeenkomsten met eiwitten in andere coronavirussen, zoals verkoudheidsvirussen. Afweerreacties hiertegen kunnen leiden tot kruisimmuniteit door antistoffen of cellulaire afweer. Dit is een mogelijk verklaring waarom kinderen, die vaak verkouden zijn, minder vaak ziek worden van SARS-2. Opvallend, kinderen hebben zelden antistoffen tegen SARS-2. Het Spike eiwit dat in de vaccins gebruikt wordt, verschilt zo sterk tussen coronavirussen dat hier geen kruisimmuniteit te verwachten is.
De sterkste afweerreactie is tegen het Spike eiwit. Na infectie zijn mensen slechts korte tijd immuun tegen corona verkoudheidsvirussen en kunnen binnen opnieuw ziek worden van hetzelfde virus. Mogelijk verspreiden neutraliserende antistoffen het virus door het lichaam. Bij een SARS-1 werd verergering van longziekte gezien na blootstelling met virus.
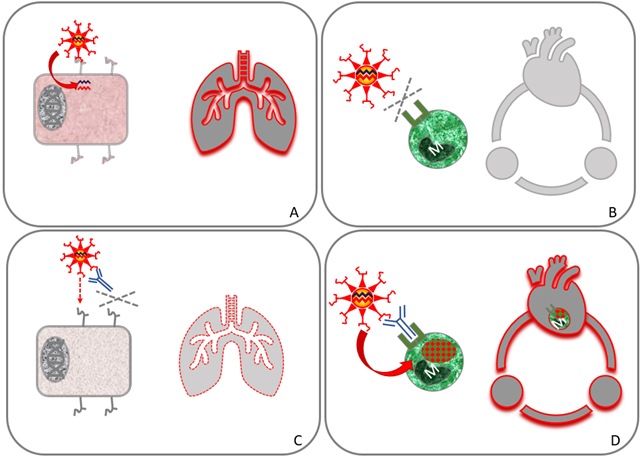
Figuur 5 Versterking infectie door antistoffen (ADE).
Alle figuren tonen links de effecten op cellulair niveau en rechts op orgaan niveau. Voor (A) en (C) in de longen en voor (B) en (D) in de circulatie. (A) In personen zonder neutraliserende antistoffen infecteert SARS-2 virus longcellen efficiënt. (B) Infectie van witte bloedcellen zoals macrofagen/monocyten [M] is niet mogelijk, omdat hiervoor geen receptor is. (C) De situatie verandert als iemand antistoffen heeft tegen het Spike eiwit van SARS-2. Dit kan in een latere fase van de ziekte zijn, bij herhaalde infectie en na antistoffen door vaccinatie. Antistoffen bemoeilijken infectie van longcellen, waardoor longziekte kan afnemen. (D) Antistoffen binden aan SARS-2 en ook aan de macrofaag. De antistof fungeert als een virusreceptor van de macrofaag die geïnfecteerd wordt. Geïnfecteerde macrofagen circuleren door het gehele lichaam en verspreiden zo het SARS-2 virus. Het virus en virusinfectie is aangegeven met rood.
Alle figuren tonen links de effecten op cellulair niveau en rechts op orgaan niveau. Voor (A) en (C) in de longen en voor (B) en (D) in de circulatie. (A) In personen zonder neutraliserende antistoffen infecteert SARS-2 virus longcellen efficiënt. (B) Infectie van witte bloedcellen zoals macrofagen/monocyten [M] is niet mogelijk, omdat hiervoor geen receptor is. (C) De situatie verandert als iemand antistoffen heeft tegen het Spike eiwit van SARS-2. Dit kan in een latere fase van de ziekte zijn, bij herhaalde infectie en na antistoffen door vaccinatie. Antistoffen bemoeilijken infectie van longcellen, waardoor longziekte kan afnemen. (D) Antistoffen binden aan SARS-2 en ook aan de macrofaag. De antistof fungeert als een virusreceptor van de macrofaag die geïnfecteerd wordt. Geïnfecteerde macrofagen circuleren door het gehele lichaam en verspreiden zo het SARS-2 virus. Het virus en virusinfectie is aangegeven met rood.
John Jacobs
28 november 2020
28 november 2020